دوره 34، شماره 12 - ( اسفند 1402 )
جلد 34 شماره 12 صفحات 759-753 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
khakzad Z, ghazavi A, abdi A, Abbasi E. INVESTIGATION THE IQ OF CHILDREN OVER 5 YEARS OLD WITH PHENYLKETONURIA, IDENTIFIED IN THE NATIONAL SCREENING PROGRAMS. Studies in Medical Sciences 2024; 34 (12) :753-759
URL: http://umj.umsu.ac.ir/article-1-6142-fa.html
URL: http://umj.umsu.ac.ir/article-1-6142-fa.html
خاکزاد زهرا، قضاوی احد، عبدی علیرضا، عباسی عزت الله. بررسی ضریب هوشی کودکان فنیلکتونوری شناساییشده در برنامه کشوری غربالگری PKU بالای 5 سال. مجله مطالعات علوم پزشکی. 1402; 34 (12) :753-759
دانشیار مغز و اعصاب کودکان، گروه بیماریهای کودکان، دانشکده پزشکی، مرکز تحقیقات نوروفیزیولوژی، پژوهشکده پزشکی سلولی و مولکولی، دانشگاه علوم پزشکی ارومیه، ارومیه، ایران (نویسنده مسئول) ، ghazavi.a@umsu.ac.ir
متن کامل [PDF 365 kb]
(372 دریافت)
| چکیده (HTML) (1251 مشاهده)
.PNG)
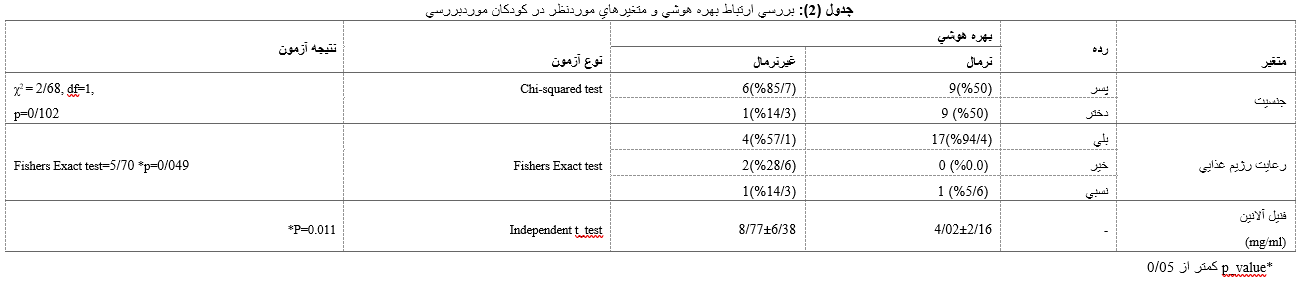
توزیع فراوانی جنسیت و بهره هوشی در کودکان با استفاده از آزمون کای 2 بررسی شد. نتایج نشان داد تفاوت آماری معنیدار بین جنسیت و بهره هوشی وجود ندارد (χ2 =2.68, df=1, p=0.102).
همچنین توزیع فراوانی رعایت رژیم غذایی و بهره هوشی در کودکان با استفاده از آزمون دقیق فیشر بررسی شد. نتایج نشان داد ارتباط آماری معنیدار بین رعایت رژیم غذایی و بهره هوشی وجود دارد.
(Fishers Exact test=5.70, p=0.049).
میانگین سطح فنیل آلانین در افراد با بهره هوشی نرمال برابر 16/2±02/4 و در افراد با بهره هوشی غیر نرمال برابر 38/6±77/8 بود، میانگین سن در دو گروه مقایسه با استفاده از آزمون t-test برای دو گروه مستقل بررسی شد، نتایج نشان داد بین میانگین سطح فنیل آلانین در افراد با بهره هوشی نرمال و غیرنرمال تفاوت آماری معنیدار وجود دارد (011/0 p=). نتایج مقایسات در جدول 2 خلاصه شده است.
متن کامل: (501 مشاهده)
مقدمه
فنیلکتونوری ([1]PKU) یکی از شایعترین خطاهای بیماریهای ارثی است که در اثر جهشهای ژن رمزگذار آنزیم فنیلالانین هیدروکسیلاز ([2]PAH) ایجاد میشود(1). PAH آنزیمی کبدی است که مسئول تبدیل فنیل آلانین، یکی از آمینواسیدهای ضروری، به تیروزین است. بهطورکلی، مسیر PAH مسئول دفع 75درصد از فنیل آلانین موجود در رژیم غذایی است و 25 فنیل آلانین باقیمانده برای سنتز پروتئین استفاده میشود. نقص فعالیت PAH منجر به افزایش سطح فنیل آلانین و متابولیتهای آن، یعنی فنیل استات و فنیل لاکتات، در خون و ادرار میشود. محدودهی طبیعی فنیل آلانین در خون110-50 میکرومول بر لیتر است(2). فقدان کامل فعالیت آنزیمی منجر به PKU کلاسیک میشود که غلظت پلاسمایی فنیل آلانین سرم در یک نوزاد تازه متولدشده قبل از درمان به بیش از 20 میلیگرم در دسی لیتر میرسد. فعالیت نسبی آنزیم باعث PKU خفیف یا متوسط، هایپرفنیلانینمی خفیف و PAH خفیف خوشخیم میشود که مورد اخیر، نیاز به درمان ندارد(3).
نوزادان تازه متولدشده با PKU در ابتدا بدون علامت هستند. با شروع تغذیه با منابع غذایی حاوی فنیل آلانین، ازجمله شیر مادر و شیر خشک معمولی، افزایش تجمع فنیل آلانین و متابولیتهای آن در بدن منجر به شروع تدریجی PKU و تظاهر خصوصیات بالینی این بیماری میشود. PKU درمان نشده باعث نقص ذهنی پیشرونده و برگشتناپذیر میشود. ضریب هوشی یک متغیر پیامد مهم برای نظارت بر رشد شناختی، ارزیابی پاسخ به درمان و تدوین دستورالعملهای درمانی برای افراد مبتلا به PKU بوده است(4).
در سال 2012، آژانس تحقیقات و کیفیت بهداشت (AHRQ) ایالاتمتحده امریکا، متاآنالیزی 17 مطالعهای (شامل 432 فرد مبتلا به PKU) را منتشر کرد که به بررسی رابطه فنیل آلانین خون با ضریب هوشی بیماران فنیلکتونوری پرداخته بود. نتایج این متاآنالیز نشان داد احتمال ضریب هوشی پایین در سطوح بالاتر فنیل آلانین خون افزایش پیدا میکند و ارتباط قویتری بین سطح فنیل آلانین اندازهگیری شده در اوایل کودکی و ضریب هوشی در سالهای بعدی زندگی وجود دارد(5). رسیدن به ضریب هوشی مناسب در افراد مبتلا به PKU به عواملی مانند سن اجرای رژیم غذایی و قطع آن و همچنین سطح PAHدر دورههای حساس رشد مرتبط است(6). در گذشته، سطح فنیل آلانین فقط در 6 سال اول زندگی (دوره بحرانی) از نزدیک کنترل میشد زیرا اعتقاد بر این بود که با بالا رفتن سن افراد تحمل بیشتری برای فنیلالانین بالا دارند(7). بهمرور ثابت شد، تأثیرات سطح بالای فنیل آلانین در رشد عصبی فراتر از اوایل کودکی بوده و حتی تا دوره بلوغ و اوایل زندگی بزرگسالی نیز گسترش مییابد(7). با توجه میزان بروز بیماری فنیلکتونوری در ایران، برنامه جامع غربالگری فنیلکتونوری، همزمان با غربالگری کمکاری مادرزادی تیروئید نوزادان در کلیه نوزادان 3 تا 5 روزه با گرفتن نمونه خون از پاشنه پا انجام میشود و در صورت مشکوک بودن (فنیلالانین بالاتر از 4 میلیگرم بر دسی لیتر)، نوزادان فراخوان شده و پس از انجام آزمایش تائید و تشخیص بیماری، بهمنظور پیشگیری از ایجاد عوارض تحت رژیم غذایی و درمان قرار میگیرند(8). اهمیت عوارض pku که مهمترین آن عقبماندگی ذهنی و عواقب و شدت آن بر جامعه است و نتایج مطالعات مختلف که ارتباط بین pku و ضریب هوشی را نشان میدهد، یکی از راهکارها لزوم پایش بیماران pku برای پیشگیری از عوارض طولانیمدت و عقبماندگی ذهنی است. با توجه به هزینههای صرف شده نظام سلامت در موردpku در سطح جامعه، نیاز به بررسی مطالعات و ارزیابی اثربخشی آن ضروری به نظر میرسد که در این راستا مطالعه حاضر باهدف بررسی ضریب هوشی کودکان فنیلکتونوری شناساییشده در برنامه کشوری غربالگری PKU کودکان بالای 5 سال انجام گردید.
مواد و روشها
در این مطالعه مقطعی-توصیفی 25 کودکان فنیلکتونوری بزرگتر از 5 سال شناساییشده در برنامه کشوری غربالگری مراجعهکننده به مرکز درمانی شهید مطهری شهرستان ارومیه در بین سالهای 1401-1391 که تحت درمان با رژیم غذایی که باعث کنترل سطح فتیل آلانین (برنامه کشوری کنترل PKU) بودند، با روش تمام شماری وارد مطالعه شدند و اطلاعات موردنیاز شامل سن، جنسیت، سطح فنیل آلانین و سن تشخیص بیماری کودک از پرونده بیماران استخراج و در چکلیست ثبت و مورد تجزیهوتحلیل قرار گرفت شد.
والدین به روانشناس ارجاع و دادهها با رعایت امانت و بدون ذکر نام بیماران جهت انجام آنالیز جمعآوری گردید. برای اندازهگیری وضعیت هوش بیماران، از پرسشنامههای سنجش هوش (Raven) برای کودکان گروه سنی 5 تا 9 سال و آزمون هوشی ریون بالغین برای گروه سنی 9 تا 16 سال مورداستفاده قرار گرفت. مبتلایان در مدتزمان 30 دقیقهای به سؤالات آزمون پاسخ دادند. نتیجه آزمون برای هر کودک ثبت و ضریب هوشی کودکان در 2 دسته نرمال (نمره 89 و بالاتر) و غیر نرمال (نمره کمتر از 88) دستهبندی شد. سطح فنیل آلانین نرمال برای کودکان کمتر از 12 سال 6-2 و برای کودکان بزرگتر از 12 سال 2-10 تعیین شد. این طرح با کد اخلاق IR.UMSU.REC.1400.404 در دانشگاه علوم پزشکی ارومیه تصویب شده است.
تمامی تحلیلها با استفاده از نرمافزار SPSS نسخه 16 انجام و سطح معنیداری برای کلیه آزمونها کمتر از 0.05 در نظر گرفته شد (p<0.05). در ابتدا برای متغیرهای کمی شاخصهای مرکزی و پراکندگی (میانگین و انحراف معیار) و برای متغیرهای کیفی فراوانی و درصد فراوانی نسبی محاسبه شدند و برای تحلیل و بررسی روابط بین متغیرها در ابتدا توزیع دادهها از آزمونهای آماری مناسب مانند independent-t-test, Fishers Exact test, Chi square استفاده گردید.
یافتهها
یافتهها نشان داد، میانگین سن کودکان موردمطالعه 44/1±32/6 سال و (60%)15 کودک موردمطالعه پسر بودند. میانگین سن تشخیص بیماری 24/52±28/30 روز و اکثریت موارد موردبررسی (84%)21 رژیم غذایی برنامه کشوری کنترل pkd را رعایت کرده بودند. میانگین سطح فنیل آلانین 33/4±40/5 و (60%)15 نفر فنیل الانین کنترل شده داشتند. میانگین بهره هوشی 99/12±56/93 به دست آمد که نشان داد (72%)18 نفر بهره هوشی متوسط به بالا دارند (جدول 1).
فنیلکتونوری ([1]PKU) یکی از شایعترین خطاهای بیماریهای ارثی است که در اثر جهشهای ژن رمزگذار آنزیم فنیلالانین هیدروکسیلاز ([2]PAH) ایجاد میشود(1). PAH آنزیمی کبدی است که مسئول تبدیل فنیل آلانین، یکی از آمینواسیدهای ضروری، به تیروزین است. بهطورکلی، مسیر PAH مسئول دفع 75درصد از فنیل آلانین موجود در رژیم غذایی است و 25 فنیل آلانین باقیمانده برای سنتز پروتئین استفاده میشود. نقص فعالیت PAH منجر به افزایش سطح فنیل آلانین و متابولیتهای آن، یعنی فنیل استات و فنیل لاکتات، در خون و ادرار میشود. محدودهی طبیعی فنیل آلانین در خون110-50 میکرومول بر لیتر است(2). فقدان کامل فعالیت آنزیمی منجر به PKU کلاسیک میشود که غلظت پلاسمایی فنیل آلانین سرم در یک نوزاد تازه متولدشده قبل از درمان به بیش از 20 میلیگرم در دسی لیتر میرسد. فعالیت نسبی آنزیم باعث PKU خفیف یا متوسط، هایپرفنیلانینمی خفیف و PAH خفیف خوشخیم میشود که مورد اخیر، نیاز به درمان ندارد(3).
نوزادان تازه متولدشده با PKU در ابتدا بدون علامت هستند. با شروع تغذیه با منابع غذایی حاوی فنیل آلانین، ازجمله شیر مادر و شیر خشک معمولی، افزایش تجمع فنیل آلانین و متابولیتهای آن در بدن منجر به شروع تدریجی PKU و تظاهر خصوصیات بالینی این بیماری میشود. PKU درمان نشده باعث نقص ذهنی پیشرونده و برگشتناپذیر میشود. ضریب هوشی یک متغیر پیامد مهم برای نظارت بر رشد شناختی، ارزیابی پاسخ به درمان و تدوین دستورالعملهای درمانی برای افراد مبتلا به PKU بوده است(4).
در سال 2012، آژانس تحقیقات و کیفیت بهداشت (AHRQ) ایالاتمتحده امریکا، متاآنالیزی 17 مطالعهای (شامل 432 فرد مبتلا به PKU) را منتشر کرد که به بررسی رابطه فنیل آلانین خون با ضریب هوشی بیماران فنیلکتونوری پرداخته بود. نتایج این متاآنالیز نشان داد احتمال ضریب هوشی پایین در سطوح بالاتر فنیل آلانین خون افزایش پیدا میکند و ارتباط قویتری بین سطح فنیل آلانین اندازهگیری شده در اوایل کودکی و ضریب هوشی در سالهای بعدی زندگی وجود دارد(5). رسیدن به ضریب هوشی مناسب در افراد مبتلا به PKU به عواملی مانند سن اجرای رژیم غذایی و قطع آن و همچنین سطح PAHدر دورههای حساس رشد مرتبط است(6). در گذشته، سطح فنیل آلانین فقط در 6 سال اول زندگی (دوره بحرانی) از نزدیک کنترل میشد زیرا اعتقاد بر این بود که با بالا رفتن سن افراد تحمل بیشتری برای فنیلالانین بالا دارند(7). بهمرور ثابت شد، تأثیرات سطح بالای فنیل آلانین در رشد عصبی فراتر از اوایل کودکی بوده و حتی تا دوره بلوغ و اوایل زندگی بزرگسالی نیز گسترش مییابد(7). با توجه میزان بروز بیماری فنیلکتونوری در ایران، برنامه جامع غربالگری فنیلکتونوری، همزمان با غربالگری کمکاری مادرزادی تیروئید نوزادان در کلیه نوزادان 3 تا 5 روزه با گرفتن نمونه خون از پاشنه پا انجام میشود و در صورت مشکوک بودن (فنیلالانین بالاتر از 4 میلیگرم بر دسی لیتر)، نوزادان فراخوان شده و پس از انجام آزمایش تائید و تشخیص بیماری، بهمنظور پیشگیری از ایجاد عوارض تحت رژیم غذایی و درمان قرار میگیرند(8). اهمیت عوارض pku که مهمترین آن عقبماندگی ذهنی و عواقب و شدت آن بر جامعه است و نتایج مطالعات مختلف که ارتباط بین pku و ضریب هوشی را نشان میدهد، یکی از راهکارها لزوم پایش بیماران pku برای پیشگیری از عوارض طولانیمدت و عقبماندگی ذهنی است. با توجه به هزینههای صرف شده نظام سلامت در موردpku در سطح جامعه، نیاز به بررسی مطالعات و ارزیابی اثربخشی آن ضروری به نظر میرسد که در این راستا مطالعه حاضر باهدف بررسی ضریب هوشی کودکان فنیلکتونوری شناساییشده در برنامه کشوری غربالگری PKU کودکان بالای 5 سال انجام گردید.
مواد و روشها
در این مطالعه مقطعی-توصیفی 25 کودکان فنیلکتونوری بزرگتر از 5 سال شناساییشده در برنامه کشوری غربالگری مراجعهکننده به مرکز درمانی شهید مطهری شهرستان ارومیه در بین سالهای 1401-1391 که تحت درمان با رژیم غذایی که باعث کنترل سطح فتیل آلانین (برنامه کشوری کنترل PKU) بودند، با روش تمام شماری وارد مطالعه شدند و اطلاعات موردنیاز شامل سن، جنسیت، سطح فنیل آلانین و سن تشخیص بیماری کودک از پرونده بیماران استخراج و در چکلیست ثبت و مورد تجزیهوتحلیل قرار گرفت شد.
والدین به روانشناس ارجاع و دادهها با رعایت امانت و بدون ذکر نام بیماران جهت انجام آنالیز جمعآوری گردید. برای اندازهگیری وضعیت هوش بیماران، از پرسشنامههای سنجش هوش (Raven) برای کودکان گروه سنی 5 تا 9 سال و آزمون هوشی ریون بالغین برای گروه سنی 9 تا 16 سال مورداستفاده قرار گرفت. مبتلایان در مدتزمان 30 دقیقهای به سؤالات آزمون پاسخ دادند. نتیجه آزمون برای هر کودک ثبت و ضریب هوشی کودکان در 2 دسته نرمال (نمره 89 و بالاتر) و غیر نرمال (نمره کمتر از 88) دستهبندی شد. سطح فنیل آلانین نرمال برای کودکان کمتر از 12 سال 6-2 و برای کودکان بزرگتر از 12 سال 2-10 تعیین شد. این طرح با کد اخلاق IR.UMSU.REC.1400.404 در دانشگاه علوم پزشکی ارومیه تصویب شده است.
تمامی تحلیلها با استفاده از نرمافزار SPSS نسخه 16 انجام و سطح معنیداری برای کلیه آزمونها کمتر از 0.05 در نظر گرفته شد (p<0.05). در ابتدا برای متغیرهای کمی شاخصهای مرکزی و پراکندگی (میانگین و انحراف معیار) و برای متغیرهای کیفی فراوانی و درصد فراوانی نسبی محاسبه شدند و برای تحلیل و بررسی روابط بین متغیرها در ابتدا توزیع دادهها از آزمونهای آماری مناسب مانند independent-t-test, Fishers Exact test, Chi square استفاده گردید.
یافتهها
یافتهها نشان داد، میانگین سن کودکان موردمطالعه 44/1±32/6 سال و (60%)15 کودک موردمطالعه پسر بودند. میانگین سن تشخیص بیماری 24/52±28/30 روز و اکثریت موارد موردبررسی (84%)21 رژیم غذایی برنامه کشوری کنترل pkd را رعایت کرده بودند. میانگین سطح فنیل آلانین 33/4±40/5 و (60%)15 نفر فنیل الانین کنترل شده داشتند. میانگین بهره هوشی 99/12±56/93 به دست آمد که نشان داد (72%)18 نفر بهره هوشی متوسط به بالا دارند (جدول 1).
.PNG)
توزیع فراوانی جنسیت و بهره هوشی در کودکان با استفاده از آزمون کای 2 بررسی شد. نتایج نشان داد تفاوت آماری معنیدار بین جنسیت و بهره هوشی وجود ندارد (χ2 =2.68, df=1, p=0.102).
همچنین توزیع فراوانی رعایت رژیم غذایی و بهره هوشی در کودکان با استفاده از آزمون دقیق فیشر بررسی شد. نتایج نشان داد ارتباط آماری معنیدار بین رعایت رژیم غذایی و بهره هوشی وجود دارد.
(Fishers Exact test=5.70, p=0.049).
میانگین سطح فنیل آلانین در افراد با بهره هوشی نرمال برابر 16/2±02/4 و در افراد با بهره هوشی غیر نرمال برابر 38/6±77/8 بود، میانگین سن در دو گروه مقایسه با استفاده از آزمون t-test برای دو گروه مستقل بررسی شد، نتایج نشان داد بین میانگین سطح فنیل آلانین در افراد با بهره هوشی نرمال و غیرنرمال تفاوت آماری معنیدار وجود دارد (011/0 p=). نتایج مقایسات در جدول 2 خلاصه شده است.

بحث و نتیجهگیری
در این مطالعه به بررسی ضریب هوشی کودکان فنیل کتونوری شناساییشده در برنامه غربالگری PKU بالای 5 سال در بیماران مراجعهکننده به مرکز درمانی شهید مطهری که تحت درمان با رژیم غذایی بودند پرداخته شد. میزان بروز بیماری فنیل کتونوری بر اساس مطالعات عقبماندگی شدید ناشی از این بیماری و نقص کامل آنزیم فنیل آلانین هیدروکسیلاز، شیوع بیماری 1 در 25000 است. ولی چون از دهه 1960 تاکنون تمام نوزادان ازنظر وجود بیماری PKU غربالگری میشوند، ازاینرو مواجهه با موارد دارای علامت کمتر است. بر اساس مطالعات انجامشده بروز این بیماری در کشورهای مختلف متفاوت است کمترین میزان بروز بیماری در تایلند 1 به 327،740 است و بالاترین میزان بروز این بیماری در ترکیه 1 به 2600 گزارش شده است. در ایران، طی اجرای برنامه غربالگری نوزادان در ایران بروز 1 در 6000 گزارش شده است(8).
در این مطالعه میانگین سن کودکان موردمطالعه 44/1±32/6 سال و میانگین سن تشخیص برابر 24/52±28/30 روز بود که در مطالعهای(9) میانگین سن مراجعه 19/39±91/43 ماه بود در مطالعهی دیگر انجامشده، میانگین سن تشخیصPKU 36ماه بود(10).
در مطالعه حاضر اختلاف آماری معنیداری بین میانگین سنی در گروه بهره هوشی نرمال و در گروه غیر نرمال وجود نداشت (403/0P=).
نتایج نشان داد در افراد با بهره هوشی نرمال (50%)9 و در گروه بهره هوشی غیرنرمال (3/14%)1 بیمار دختر بودند و ارتباط آماری معنیدار بین بهره هوشی دختران و پسران وجود ندارد. (102/0=P) که با نتایج سایر مطالعات همسو بود(9).
در کودکان با بهره هوشی نرمال (4/94%)17 کودک رژیم غذایی موردنظر را رعایت و در کودکان با بهره هوشی غیرنرمال (1/57%)4 کودک رژیم غذایی را رعایت کرده بودند. ارتباط آماری معنیدار بین بهره هوشی و رعایت رژیم غذایی مشاهده شد (049/0=P). Koch و همکاران با بررسی بیماران با درمان دیرهنگام گزارش کرد، میانگین بهره هوشی در افرادی که رژیم غذایی را بهطور مرتب رعایت نکردهاند بالاتر از افرادی است که آن را بهخوبی رعایت کردهاند(10). مطالعه پوتنسیک و همکاران در استرالیا نیز نشان داد آن دسته از بیمارانی که رژیم غذایی خود را بهطور کامل تا 10 سالگی رعایت میکنند دچار نقایص عصبی کمتری میباشند. بااینحال حتی در بهترین شرایط اغلب این بیماران در زمان ورود به مدرسه نسبت به خواهران و برادران سالم خود از ضریب هوشی پایینتری برخوردار هستند(11). Janzenو Nguyen در یک مقاله مروری گزارش کردند رعایت ضعیف رژیم و عدم ادامه آن باعث کاهش نمرات هوش خواهد شد(12).
در مطالعه ما میانگین فنیل آلانین در گروه بهره هوشی نرمال برابر 16/2±02/4 و در گروه غیر نرمال برابر 38/6±77/8 بود، که ازنظر آماری این اختلاف معنیداری بود (011/0P=). در مطالعات Michel و همکاران همبستگی منفی بین بهره هوشی و میزان فتیل آلانین خون گزارش شده است(13-17). در مطالعهای که Diamond و همکاران روی 148 کودک ششماهه تا هفتساله مبتلا به فنیل کتونوری زود درمــان شـده انجـام داد، گزارش کرد کودکانی که ســطح فنیل آلانیـن خونشـان همزمان بــا اجـرای آزمونها در محـدودە L / µmol360-600 بـوده اسـت، نسـبت بـه کودکـانی کـه سـطح فنیل آلانیـن آنها کمتر ازL / µmol360 بود، در اجرای آزمونهای اجرایــی (حافظـه کـاری و کنترل مهاری) نتایج ضعیفتری کسب کردهاند(35). در مطالعـه لوسـیانا و همکـاران و ولگیـج و همکـــاران بین میانگین سطح فنیل آلانین در طول زندگی افراد مبتلا به فنیل کتونوری تحت درمان و بهره هوشی ارتباط معنیدار مشــاهده شـد. بهاینترتیب که افزایش سطح فنیل آلانین با بهره هوشی کمتر همراه بود(18, 19).
نتایج کاربردی:
به نظر میرسد برنامه غربالگری pku در استان آذربایجان غربی اثربخشی لازم را داشته و شاهد کاهش عوارض این بیماری بودهایم. اما باوجود پیگیریها و اجرای برنامه هنوز شاهد برخی عوارض خاص مانند عقبماندگی ذهنی هستیم (23 درصد کودکان با ضریب هوشی متوسط به پایین) که با توجه به اثرات جبرانناپذیر آن ضروری به نظر میرسد انسجام و تداوم برنامه در راستای به حداقل رساندن عوارض ناشی از این بیماری ضروری است.
نقاط قدرت و ضعف مطالعه: نتایج این مطالعه با توجه به استفاده از پرونده ثبتشده بیماران وعدم امکان بررسی جامعتر متغیرهای مؤثر دارای محدودیتهایی بوده است. اما انجام بررسیها و معاینات توسط متخصص و روانشناس و ابزار استاندارد از نقاط قوت مطالعه محسوب میشود.
پیشنهادها:
پیشنهاد میشود در برنامههای کنترلی و مراقبتی کودکان مبتلا به pku در کنار انجام بررسیهای بالینی و پاراکلینیکی مراقبتهای ادواری و کوتاهمدت توسط روانشناس و روانپزشک صورت گیرد و نیز برنامههای مبتنی بر خانواده و آموزشهای مربوطه طراحی و اجرا گردد. همچنین این مطالعه تنها به بررسی ضریب هوشی بهعنوان مؤلفهای از تکامل نورولوژیک بیمار میپردازد درحالیکه مطالعات نشان میدهد حتی بیماران فنیلکتونوری که ضریب هوشی نرمال دارند در مهارتهای هوشی اجرایی و نیز ازنظر روانشناختی در مقایسه با جمعیت نرمال مشکلات عمدهای دارند. طراحی مطالعهای در این زمینه پیشنهاد میشود.
تشکر و قدردانی:
اعلام نشده است.
حمایت مالی:
ندارد.
ملاحظات اخلاقی:
این تحقیق دارای کد اخلاق با شماره IR.UMSU.REC.1400.404 از کمیته اخلاق دانشگاه علوم پزشکی ارومیه است.
در این مطالعه به بررسی ضریب هوشی کودکان فنیل کتونوری شناساییشده در برنامه غربالگری PKU بالای 5 سال در بیماران مراجعهکننده به مرکز درمانی شهید مطهری که تحت درمان با رژیم غذایی بودند پرداخته شد. میزان بروز بیماری فنیل کتونوری بر اساس مطالعات عقبماندگی شدید ناشی از این بیماری و نقص کامل آنزیم فنیل آلانین هیدروکسیلاز، شیوع بیماری 1 در 25000 است. ولی چون از دهه 1960 تاکنون تمام نوزادان ازنظر وجود بیماری PKU غربالگری میشوند، ازاینرو مواجهه با موارد دارای علامت کمتر است. بر اساس مطالعات انجامشده بروز این بیماری در کشورهای مختلف متفاوت است کمترین میزان بروز بیماری در تایلند 1 به 327،740 است و بالاترین میزان بروز این بیماری در ترکیه 1 به 2600 گزارش شده است. در ایران، طی اجرای برنامه غربالگری نوزادان در ایران بروز 1 در 6000 گزارش شده است(8).
در این مطالعه میانگین سن کودکان موردمطالعه 44/1±32/6 سال و میانگین سن تشخیص برابر 24/52±28/30 روز بود که در مطالعهای(9) میانگین سن مراجعه 19/39±91/43 ماه بود در مطالعهی دیگر انجامشده، میانگین سن تشخیصPKU 36ماه بود(10).
در مطالعه حاضر اختلاف آماری معنیداری بین میانگین سنی در گروه بهره هوشی نرمال و در گروه غیر نرمال وجود نداشت (403/0P=).
نتایج نشان داد در افراد با بهره هوشی نرمال (50%)9 و در گروه بهره هوشی غیرنرمال (3/14%)1 بیمار دختر بودند و ارتباط آماری معنیدار بین بهره هوشی دختران و پسران وجود ندارد. (102/0=P) که با نتایج سایر مطالعات همسو بود(9).
در کودکان با بهره هوشی نرمال (4/94%)17 کودک رژیم غذایی موردنظر را رعایت و در کودکان با بهره هوشی غیرنرمال (1/57%)4 کودک رژیم غذایی را رعایت کرده بودند. ارتباط آماری معنیدار بین بهره هوشی و رعایت رژیم غذایی مشاهده شد (049/0=P). Koch و همکاران با بررسی بیماران با درمان دیرهنگام گزارش کرد، میانگین بهره هوشی در افرادی که رژیم غذایی را بهطور مرتب رعایت نکردهاند بالاتر از افرادی است که آن را بهخوبی رعایت کردهاند(10). مطالعه پوتنسیک و همکاران در استرالیا نیز نشان داد آن دسته از بیمارانی که رژیم غذایی خود را بهطور کامل تا 10 سالگی رعایت میکنند دچار نقایص عصبی کمتری میباشند. بااینحال حتی در بهترین شرایط اغلب این بیماران در زمان ورود به مدرسه نسبت به خواهران و برادران سالم خود از ضریب هوشی پایینتری برخوردار هستند(11). Janzenو Nguyen در یک مقاله مروری گزارش کردند رعایت ضعیف رژیم و عدم ادامه آن باعث کاهش نمرات هوش خواهد شد(12).
در مطالعه ما میانگین فنیل آلانین در گروه بهره هوشی نرمال برابر 16/2±02/4 و در گروه غیر نرمال برابر 38/6±77/8 بود، که ازنظر آماری این اختلاف معنیداری بود (011/0P=). در مطالعات Michel و همکاران همبستگی منفی بین بهره هوشی و میزان فتیل آلانین خون گزارش شده است(13-17). در مطالعهای که Diamond و همکاران روی 148 کودک ششماهه تا هفتساله مبتلا به فنیل کتونوری زود درمــان شـده انجـام داد، گزارش کرد کودکانی که ســطح فنیل آلانیـن خونشـان همزمان بــا اجـرای آزمونها در محـدودە L / µmol360-600 بـوده اسـت، نسـبت بـه کودکـانی کـه سـطح فنیل آلانیـن آنها کمتر ازL / µmol360 بود، در اجرای آزمونهای اجرایــی (حافظـه کـاری و کنترل مهاری) نتایج ضعیفتری کسب کردهاند(35). در مطالعـه لوسـیانا و همکـاران و ولگیـج و همکـــاران بین میانگین سطح فنیل آلانین در طول زندگی افراد مبتلا به فنیل کتونوری تحت درمان و بهره هوشی ارتباط معنیدار مشــاهده شـد. بهاینترتیب که افزایش سطح فنیل آلانین با بهره هوشی کمتر همراه بود(18, 19).
نتایج کاربردی:
به نظر میرسد برنامه غربالگری pku در استان آذربایجان غربی اثربخشی لازم را داشته و شاهد کاهش عوارض این بیماری بودهایم. اما باوجود پیگیریها و اجرای برنامه هنوز شاهد برخی عوارض خاص مانند عقبماندگی ذهنی هستیم (23 درصد کودکان با ضریب هوشی متوسط به پایین) که با توجه به اثرات جبرانناپذیر آن ضروری به نظر میرسد انسجام و تداوم برنامه در راستای به حداقل رساندن عوارض ناشی از این بیماری ضروری است.
نقاط قدرت و ضعف مطالعه: نتایج این مطالعه با توجه به استفاده از پرونده ثبتشده بیماران وعدم امکان بررسی جامعتر متغیرهای مؤثر دارای محدودیتهایی بوده است. اما انجام بررسیها و معاینات توسط متخصص و روانشناس و ابزار استاندارد از نقاط قوت مطالعه محسوب میشود.
پیشنهادها:
پیشنهاد میشود در برنامههای کنترلی و مراقبتی کودکان مبتلا به pku در کنار انجام بررسیهای بالینی و پاراکلینیکی مراقبتهای ادواری و کوتاهمدت توسط روانشناس و روانپزشک صورت گیرد و نیز برنامههای مبتنی بر خانواده و آموزشهای مربوطه طراحی و اجرا گردد. همچنین این مطالعه تنها به بررسی ضریب هوشی بهعنوان مؤلفهای از تکامل نورولوژیک بیمار میپردازد درحالیکه مطالعات نشان میدهد حتی بیماران فنیلکتونوری که ضریب هوشی نرمال دارند در مهارتهای هوشی اجرایی و نیز ازنظر روانشناختی در مقایسه با جمعیت نرمال مشکلات عمدهای دارند. طراحی مطالعهای در این زمینه پیشنهاد میشود.
تشکر و قدردانی:
اعلام نشده است.
حمایت مالی:
ندارد.
ملاحظات اخلاقی:
این تحقیق دارای کد اخلاق با شماره IR.UMSU.REC.1400.404 از کمیته اخلاق دانشگاه علوم پزشکی ارومیه است.
نوع مطالعه: پژوهشي(توصیفی- تحلیلی) |
موضوع مقاله:
اعصاب کودکان
فهرست منابع
1. Flydal MI, Martinez A. Phenylalanine hydroxylase: function, structure, and regulation. IUBMB Life 2013;65(4):341-9. http://dx.doi.org/10.1002/iub.1150 [DOI:10.1002/iub.1150] [PMID]
2. Herenger Y, Maes E, François L, Pasco J, Bouchereau J, Pichard S, et al. Determining factors of the cognitive outcome in early treated PKU: A study of 39 pediatric patients. Mol Genet Metab Rep 2019;20(100498):100498. http://dx.doi.org/10.1016/j.ymgmr.2019.100498 [DOI:10.1016/j.ymgmr.2019.100498] [PMID] []
3. van Spronsen FJ, Blau N, Harding C, Burlina A, Longo N, Bosch AM. Phenylketonuria. Nat Rev Dis Primers 2021;7(1):36. http://dx.doi.org/10.1038/s41572-021-00267-0 [DOI:10.1038/s41572-021-00267-0] [PMID] []
4. Moyle JJ, Fox AM, Arthur M, Bynevelt M, Burnett JR. Meta-analysis of neuropsychological symptoms of adolescents and adults with PKU. Neuropsychol Rev 2007;17(2):91-101. http://dx.doi.org/10.1007/s11065-007-9021-2 [DOI:10.1007/s11065-007-9021-2] [PMID]
5. Burgard P. Development of intelligence in early treated phenylketonuria. Eur J Pediatr 2000;159 Suppl 2:S74-9. http://dx.doi.org/10.1007/pl00014388 [DOI:10.1007/PL00014388] [PMID]
6. Fonnesbeck CJ, McPheeters ML, Krishnaswami S, Lindegren ML, Reimschisel T. Estimating the probability of IQ impairment from blood phenylalanine for phenylketonuria patients: a hierarchical meta-analysis. J Inherit Metab Dis 2013;36(5):757-66. http://dx.doi.org/10.1007/s10545-012-9564-0 [DOI:10.1007/s10545-012-9564-0] [PMID]
7. Koch R, Burton B, Hoganson G, Peterson R, Rhead W, Rouse B, et al. Phenylketonuria in adulthood: A collaborative study. J Inherit Metab Dis 2002;25(5):333-46. http://dx.doi.org/10.1023/a:1020158631102 [DOI:10.1023/A:1020158631102] [PMID]
8. Heidari A, Arab M, Etemad K, Damari B, Lotfi M. National Phenylketonuria Screening Program in Iran; Why and How? Sci J Schf Pub Health Instit Pub Health Res 2018;16(2):148-63. [Google Scholar]
9. Daneshi S, Takaloo M, Davarani R, Heidarabadi M. Rezabeigi Davarani E. Incidence of phenylketonuria and the effect of prevention national program on reducing its incidence in the population covered by Kerman University of Medical Sciences during. Iran J Obstet Gynecol Infertil 2007;24(13):59-69. [Google Scholar]
10. Sadek AA, Hassan MH, Mohammed NA. Clinical and neuropsychological outcomes for children with phenylketonuria in Upper Egypt; a single-center study over 5 years. Neuropsychiatr Dis Treat 2018;14:2551-61. http://dx.doi.org/10.2147/NDT.S176198 [DOI:10.2147/NDT.S176198] [PMID] []
11. Khemir S, Halayem S, Azzouz H, Siala H, Ferchichi M, Guedria A, et al. Autism in phenylketonuria patients: From clinical presentation to molecular defects: From clinical presentation to molecular defects. J Child Neurol 2016;31(7):843-9. http://dx.doi.org/10.1177/0883073815623636 [DOI:10.1177/0883073815623636] [PMID]
12. Saad K, Elserogy Y, Abdel Rahman AA, Al-Atram AA, Mohamad IL, ElMelegy TTH, et al. ADHD, autism and neuroradiological complications among phenylketonuric children in Upper Egypt. Acta Neurol Belg 2015;115(4):657-63. http://dx.doi.org/10.1007/s13760-014-0422-8 [DOI:10.1007/s13760-014-0422-8] [PMID]
13. Koch R, Moseley K, Ning J, Romstad A, Guldberg P, Guttler F. Long-term beneficial effects of the phenylalanine-restricted diet in late-diagnosed individuals with phenylketonuria. Mol Genet Metab 1999;67(2):148-55. http://dx.doi.org/10.1006/mgme.1999.2863 [DOI:10.1006/mgme.1999.2863] [PMID]
14. Potocnik U, Widhalm K. Long-term follow-up of children with classical phenylketonuria after diet discontinuation: a review. J Am Coll Nutr 1994;13(3):232-6. http://dx.doi.org/10.1080/07315724.1994.10718402 [DOI:10.1080/07315724.1994.10718402] [PMID]
15. Janzen D, Nguyen M. Beyond executive function: non-executive cognitive abilities in individuals with PKU. Mol Genet Metab 2010;99 Suppl 1:S47-51. http://dx.doi.org/10.1016/j.ymgme.2009.10.009 [DOI:10.1016/j.ymgme.2009.10.009] [PMID]
16. Waisbren SE, Noel K, Fahrbach K, Cella C, Frame D, Dorenbaum A, et al. Phenylalanine blood levels and clinical outcomes in phenylketonuria: a systematic literature review and meta-analysis. Mol Genet Metab 2007;92(1-2):63-70. http://dx.doi.org/10.1016/j.ymgme.2007.05.006 [DOI:10.1016/j.ymgme.2007.05.006] [PMID]
17. Michel U, Schmidt E, Batzler U. Results of psychological testing of patients aged 3-6 years. Eur J Pediatr 1990;149 Suppl 1:S34-8. http://dx.doi.org/10.1007/bf02126297 [DOI:10.1007/BF02126297] [PMID]
18. Brumm VL, Grant ML. The role of intelligence in phenylketonuria: a review of research and management. Mol Genet Metab 2010;99 Suppl 1:S18-21. http://dx.doi.org/10.1016/j.ymgme.2009.10.015 [DOI:10.1016/j.ymgme.2009.10.015] [PMID]
19. Welsh M, Deroche K, Gilliam DA. Neurocognitive models of early-treated Phenylketonuria: insights from meta-analysis and new molecular genetic findings. Handb Dev Cogne Neurosci 2008;2:677-89. [Google Scholar]
20. Ris MD, Williams SE, Hunt MM, Berry HK, Leslie N. Early-treated phenylketonuria: adult neuropsychologic outcome. J Pediatr 1994;124(3):388-92. http://dx.doi.org/10.1016/s0022-3476(94)70360-4 [DOI:10.1016/S0022-3476(94)70360-4] [PMID]
21. Luciana M, Sullivan J, Nelson CA. Associations between phenylalanine‐to‐tyrosine ratios and performance on tests of neuropsychological function in adolescents treated early and continuously for phenylketonuria. Child Dev 2001;72(6):1637-52. http://dx.doi.org/10.1111/1467-8624.00370 [DOI:10.1111/1467-8624.00370] [PMID]
22. Weglage J, Pietsch M, Fünders B, Koch H, Ullrich K. Deficits in selective and sustained attention processes in early treated children with phenylketonuria-result of impaired frontal lobe functions? Eur J Pediatr 1996;155:200-4. [DOI:10.1007/BF01953938] [PMID]
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |







